سرطان مغز استخوان، که اغلب به عنوان مالتیپل میلوما (Multiple Myeloma) شناخته میشود، نوعی سرطان خون است که از سلولهای پلاسما (نوعی گلبول سفید که آنتیبادی تولید میکند) در مغز استخوان منشأ میگیرد. این بیماری با تجمع سلولهای میلوم غیرطبیعی مشخص میشود که جایگزین سلولهای سالم خونی شده و باعث آسیب به استخوانها، کاهش ایمنی بدن و مشکلات کلیوی میشوند.
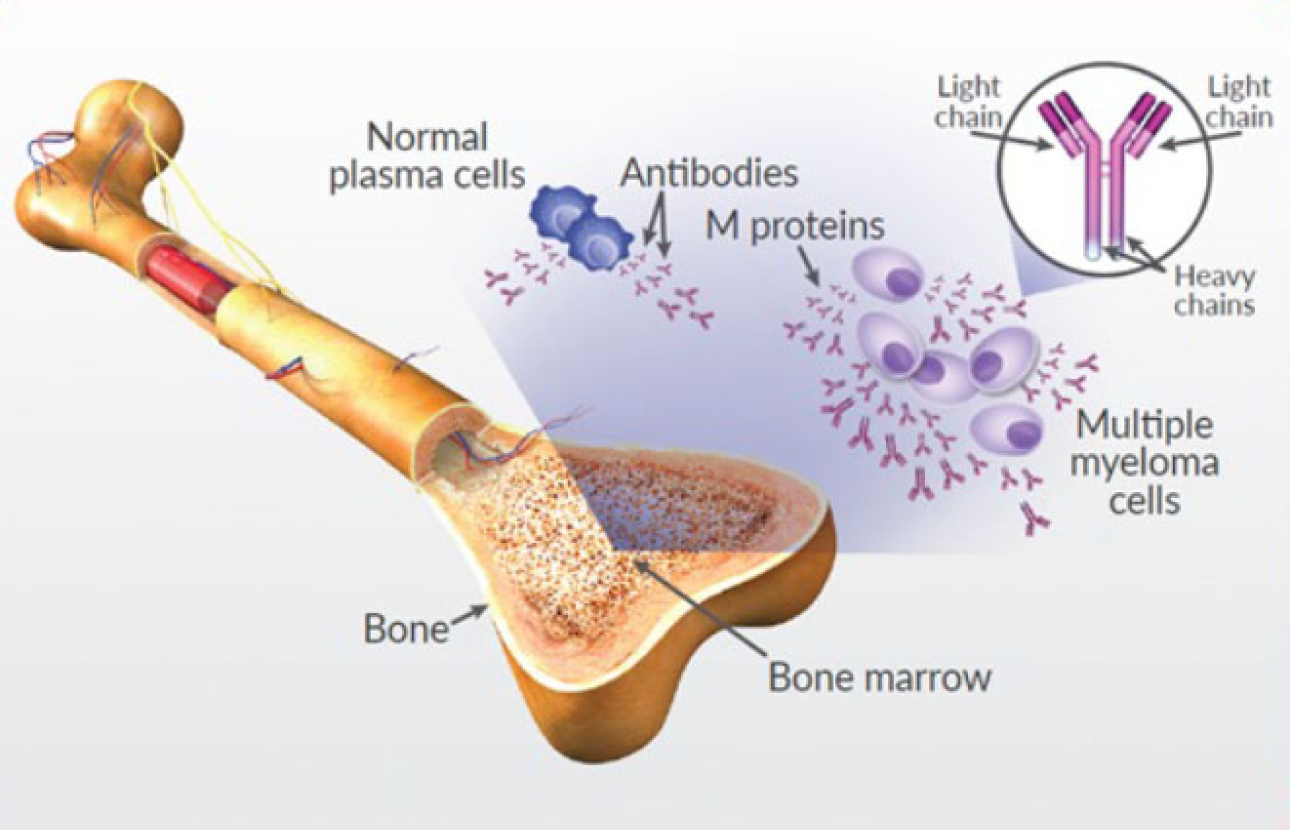
۱. دلیل پیدایش و تشخیص سرطان مغز استخوان
مالتیپل میلوما در نتیجه جهشهای ژنتیکی اکتسابی در یک سلول پلاسما در مغز استخوان ایجاد میشود. این سلول جهشیافته به طور غیرقابل کنترل تکثیر میشود و پروتئینهای غیرطبیعی به نام پروتئینهای M یا ایمونوگلوبولینهای تکتیرهای تولید میکند که در خون و ادرار تجمع مییابند.
پیامدهای اصلی بیماری:
- آسیب استخوانی (Bone Lesions): سلولهای میلوم، استئوکلاستها (سلولهای تخریبکننده استخوان) را تحریک کرده و باعث ایجاد درد استخوانی، شکستگی و افزایش سطح کلسیم خون میشوند.
- کمخونی و عفونت: تجمع سلولهای میلوم، تولید طبیعی گلبولهای قرمز و سفید را مختل کرده و منجر به کمخونی و ضعف سیستم ایمنی میشود.
- مشکلات کلیوی: پروتئینهای M میتوانند به کلیهها آسیب بزنند و باعث نارسایی کلیوی شوند.
۲. درمانهای فعلی و استاندارد مالتیپل میلوما
درمان مالتیپل میلوما معمولاً شامل ترکیبی از داروها برای کنترل بیماری، کاهش علائم و جلوگیری از پیشرفت آن است، زیرا در حال حاضر اغلب یک بیماری مزمن و نه کاملاً قابل درمان تلقی میشود.
- شیمیدرمانی و استروئیدها: برای از بین بردن سریع سلولهای میلوم استفاده میشوند.
- پیوند سلولهای بنیادی اتولوگ (Autologous SCT): پس از شیمیدرمانی با دوز بالا، سلولهای بنیادی سالم خود بیمار به او تزریق میشوند تا مغز استخوان بازسازی شود. این روش، طول مدت بهبودی را افزایش میدهد.
- داروهای تعدیلکننده سیستم ایمنی (IMiDs): داروهایی مانند تالیدومید، لنالیدومید و پومالیدومید که عملکرد سیستم ایمنی را برای مبارزه با میلوم تقویت میکنند و مستقیماً روی سلولهای میلوم اثر میگذارند.
- مهارکنندههای پروتئازوم (Proteasome Inhibitors): داروهایی مانند بورتزومیب و کارفیلزومیب که با مسدود کردن پروتئازوم (ساختاری در سلولها که پروتئینهای آسیبدیده را تجزیه میکند)، باعث تجمع پروتئینهای غیرطبیعی و مرگ سلول میلوم میشوند.
۳. تحولات اخیر و درمانهای نوین
در یک دهه اخیر، مالتیپل میلوما بیشترین تحول را در بین سرطانهای خون تجربه کرده است که منجر به افزایش چشمگیر نرخ بقا شده است.
الف) ایمونوتراپی و سلولدرمانی CAR T-Cell
این روش یکی از پیشرفتهترین درمانها برای میلوم عودکننده و مقاوم به درمان است:
- هدفگیری BCMA: اکثر درمانهای CAR T برای میلوما، پروتئین BCMA (B-cell Maturation Antigen) را که به وفور روی سلولهای میلوم وجود دارد، هدف قرار میدهند.
- عملکرد: سلولهای T بیمار مهندسی شده و به بدن بازگردانده میشوند تا سلولهای میلوم حاوی BCMA را پیدا کرده و از بین ببرند. این روش نتایج بسیار امیدوارکنندهای در بیمارانی که به داروهای استاندارد پاسخ نمیدهند، نشان داده است.
ب) آنتیبادیهای دومنظوره (Bispecific Antibodies)
- مکانیزم: این آنتیبادیها دارای دو بازوی هدفگیرنده هستند: یک بازو به سلول میلوم (مثلاً BCMA) و بازوی دیگر به سلول T بیمار (CD3) متصل میشود.
- عملکرد: آنتیبادی دومنظوره مانند یک پل عمل کرده و سلولهای T خود بیمار را مستقیماً به سمت سلولهای میلوم هدایت کرده و فعال میکند تا به سلولهای سرطانی حمله کنند. این روش، یک راهکار خارج از بدن (off-the-shelf) ارائه میدهد که سریعتر از CAR T قابل دسترسی است.
ج) داروهای هدفمند نسل سوم
- آنتیبادیهای ضد CD38: داروهایی مانند داراتوموماب که گیرنده CD38 روی سلولهای میلوم را هدف قرار میدهند و به طور مستقیم یا با فراخوانی سلولهای ایمنی، سلولهای میلوم را از بین میبرند. این داروها اکنون بخشی از خط اول درمان در بسیاری از رژیمها هستند.
۴. آینده درمان مالتیپل میلوما
آینده درمان میلوما بر حذف کامل بیماری و تبدیل آن به یک بیماری قابل مدیریت برای طولانیمدت متمرکز است:
- درمان بدون شیمیدرمانی: حرکت به سمت رژیمهای درمانی کاملاً مبتنی بر داروهای هدفمند و ایمونوتراپی برای کاهش عوارض جانبی شیمیدرمانی.
- درمان هدفمند مبتنی بر زیرگروهها: استفاده از توالییابی ژنتیکی برای شناسایی دقیق زیرگروههای مولکولی میلوم و تجویز درمانهای فوقالعاده شخصیسازیشده (مثلاً هدف قرار دادن جهشهای خاص KRAS یا BRAF).
- CAR T در مراحل اولیه: استفاده از CAR T و Bi-Specifics نه تنها به عنوان راه نجات، بلکه به عنوان بخشی از درمان اولیه برای افزایش شانس ریشهکنی بیماری.
- مدیریت بیماری باقیمانده ناچیز (MRD): هدف نهایی درمان، دستیابی به وضعیت MRD-منفی است (حتی یک سلول سرطانی در 100,000 سلول سالم در مغز استخوان قابل تشخیص نباشد). نظارت دقیق بر MRD به تعیین زمان قطع یا ادامه درمان کمک میکند و شخصیسازی نهایی را ممکن میسازد.